מעבדת בריגמן חוקרת כיצד עלבון נוירו -התפתחותי ומחלות נוירו -פסיכיאטריות מובילות לשינויים התנהגותיים לא הסתגליים המפחיתים את איכות החיים במטרה להציל את הגירעונות הללו ולשפר את התוצאות.

באופן מסורתי, מחקרים במכרסמים מנצלים התנהגויות המתמקדות בחוזקות שלהן (חפירה, ריח, ניווט). למרות שגישות אלה הניבו שפע של נתונים, הן שונות מאוד מהאופן בו אנו מודדים תפקוד קוגניטיבי בבני אדם. מטרה מרכזית של המעבדה היא לפתח ולאמת מבחנים חדשים לחקר תוצאות התנהגותיות שניתן להשוות ביתר ישירות לנתונים קליניים. החל משנת 2001 עבדתי על פיתוח ושיפור משימות תוך שימוש בגישות מסך מגע ללמידות מסך, זיכרון והתנהגויות שליטה במנהלים. עבודה זו סייעה לבסס את התועלת של העכבר במחקר תפקודי מנהלים והובילה לאימוץ רחב יותר של פרדיגמות אופרנטיות למסך מגע להקרנת תפוקה גבוהה. במשך 10 השנים האחרונות המעבדה שלי שילבה הקלטה in vivo של פעילות הנוירונים בקליפת המוח ופוטנציאל השדה המקומי במהלך משימות אלה in vivo כדי לעזור לנו להבין טוב יותר כיצד אזורי מוח שונים מתווכים התנהגויות ספציפיות. לאחרונה, היינו מעורבים במחקר רב אוניברסיטאי להשוואת פעילות עצבית הקשורה להתנהגות ספציפית אצל מכרסמים ובני אדם כאחד כדי לבדוק את התועלת של נתוני התנהגות מכרסמים בפיתוח מטרות טיפוליות.
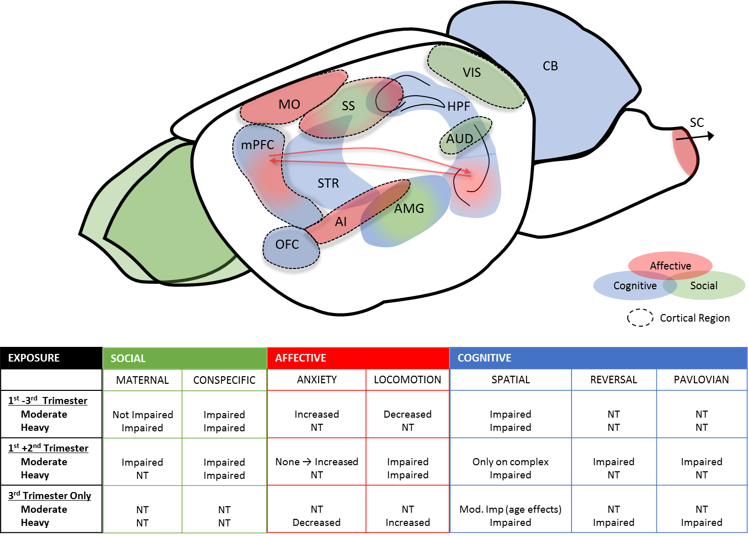
השפעת האלכוהול על תפקוד קליפת המוח ותהליכי הבקרה המבצעת העומדת בבסיסו היא סוגיה קריטית שכן אובדן תהליכים מרכזיים אלה עלול להוביל לירידה משמעותית באיכות החיים. למרות שההשפעה של חשיפה התפתחותית או מבוגרת על משימות מרחביות, ובאופן פחות אופרטיבי, תועדה היטב, מעט מחקרים השתמשו במדידה מקוונת של תפקוד עצבי כדי לנתח שינויים ברמת המעגלים לאחר החשיפה. שימוש בטכניקות in vivo טכניקות הקלטה, מעבדת בריגמן אפילו חשיפה מתונה יותר לפני הלידה מספיקה כדי לפגוע בגמישות ההתנהגותית ולשנות ירי וגיוס קליפת המוח. בנוסף, נדרשת תיאום דיסקרטי של קורטיקו-סטריאטלי של PAE לצורך גמישות התנהגותית. לאחרונה, הראינו כי PAE גם משנה את התנהגות ההחזרה והאפליה הוויזואו-מרחבית במקרים שבהם התנזרות EtOH אחרת לבגרות מוקדמת. באופן מרגש, הראינו גם כי סביבת החיים המוקדמת יכולה לשנות באופן משמעותי את התוצאות במודלים אלה.
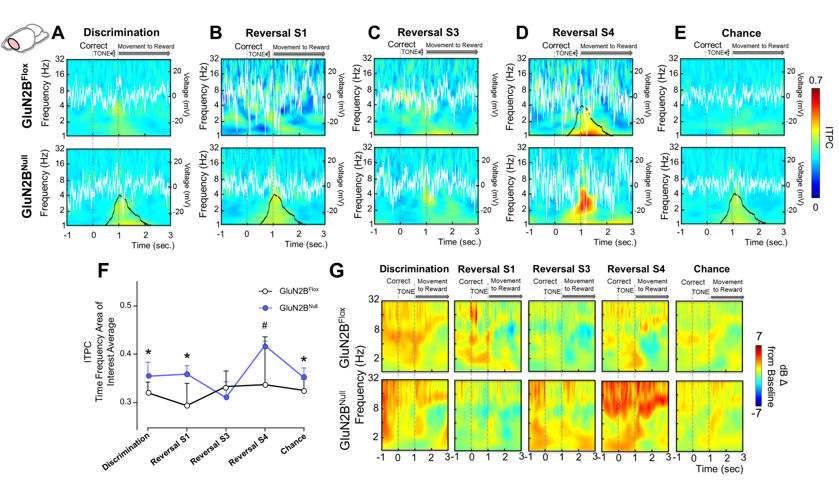
אובדן תת -סוגים ספציפיים של NMDAR בקליפת המוח, בהיפוקמפוס ובסטריאטום יכול לשנות הן למידה והן גמישות סינפטית. בהתבסס על מחקרים בסיסיים שנערכו במעבדת הולמס, המעבדה שלי חקרה את תפקידם של GluN2A ו- GluN2B המכיל NMDAR באמצעות מודלים ניקי-אאוט רחבים ומותנים על-ידי מונית והפעלה פרמקולוגית. הראינו שאובדן GluN2A מוחי פוגע בלמידה פשוטה ובגמישות במשימה משתנה. יתר על כן, הראינו כי אובדן GluN2B בקליפת המוח ובהיפוקמפוס חוסך למידת אפליה אך פוגע ביכולת ללמוד כללים מתאימים וליישם כללים אלה על בעיות חדשות. מחקרים עדכניים יותר שילבו עכברי knock-out מסוג GluN2B עם in vivo הקלטה במהלך ההתנהגות כדי להראות שאובדן יחידת המשנה משנה פעילות גופנית וקליפת המוח, ואת האופן שבו האזורים מתקשרים. בהתחשב בממצאים כי עלבונות התפתחותיים כמו חשיפה לאלכוהול טרום לידתי משנים את ביטוי יחידת המשנה של NMDAR, אנו בודקים כעת האם ביטוי זה עשוי לתווך למידה יעילה ושינוי.
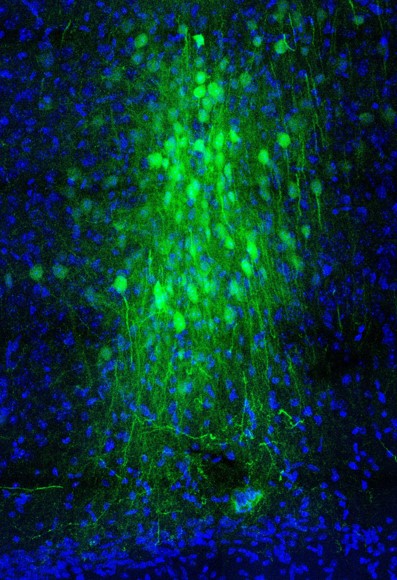
ליקויים בתפקוד הביצועי הם תכונה נפוצה בהפרעות נוירופסיכיאטריות רבות. למעשה, לליקויים קוגניטיביים עשויה להיות השפעה שלילית גדולה יותר על איכות החיים של חולי סכיזופרניה מאשר תסמינים שליליים או חיוביים. מודלים פרה -קליניים של סכיזופרניה הראו כיצד אובדן מערכות ספציפיות הוביל לפגיעה התנהגותית במשימות תרגום. בעבר, הראיתי שאובדן תפקוד GABAergic במוח הקדמי מספיק כדי לשנות את תשומת הלב ולפגוע בלמידה היפוכת בעוד שפנסיקלידין כרונית שינתה את אמצעי החקירה החברתית אך חסכה למידה והיפוך. לאחרונה, מעבדת בריגמן, בשיתוף עם מעבדת מליוס ב- UNM, הראתה כי מציאה של circHomer1a, circRNA מועשר עצבי המתבטא בקליפת המוח הקדמית, הספיק כדי לפגוע בהיפוך במשימת האפליה החזותית שלנו במסך המגע. חשוב לציין שגם מעבדת מליוס הראתה זאת circHomer1a הופחת באופן משמעותי בדגימות של רקמת PFC לאחר המוות בחולים עם סכיזופרניה והפרעה דו קוטבית. מחקרים שיתופיים נמשכים כיום חוקרים את המנגנונים כיצד שינויים ב- microRNAs מעגליים עלולים לפגוע בהתנהגות.